Marc Humbert : « On ne fait pas de la recherche médicale par hasard mais avant tout pour aider des patients, parfois très jeunes et en grande difficulté »
Marc Humbert est doyen de la faculté de médecine Paris-Saclay, chef du service de pneumologie et de soins intensifs respiratoires au centre de référence de l’hypertension pulmonaire de l’hôpital Bicêtre (AP-HP) et directeur de l’unité Inserm/université Paris-Saclay dédiée à l’hypertension pulmonaire.
Le Grand Prix Inserm 2025 vient de récompenser le Pr Marc Humbert, figure majeure de la lutte contre l’hypertension artérielle pulmonaire. À cette occasion, il a accepté de revenir sur la portée scientifique de ses travaux et sur les enjeux actuels de cette maladie rare et grave.
En quoi l’hypertension artérielle pulmonaire (HTAP) reste-t-elle particulièrement redoutable pour les patients ?
L’HTAP est une maladie rare et grave, qui touche 15 à 50 personnes pour un million. C’est une cause d’hypertension pulmonaire, un ensemble de maladies caractérisées par l’augmentation chronique de la pression au niveau des artères pulmonaires. Les autres formes d’hypertension pulmonaire sont plus fréquentes et liées à une insuffisance cardiaque, une maladie respiratoire, ou des séquelles d’embolie pulmonaire.
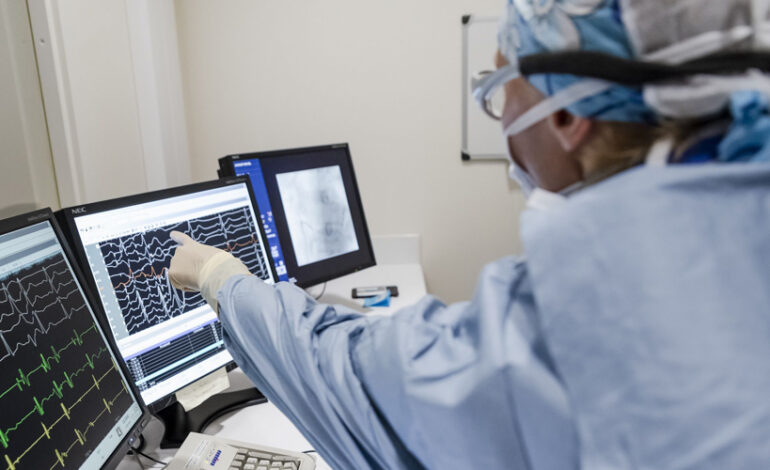
En cas d’HTAP, l’augmentation durable de la pression impose un effort excessif à la partie droite du cœur, qui n’est physiologiquement pas conçue pour pomper le sang contre une forte résistance. Cela conduit à une insuffisance cardiaque droite qui entraîne le décès. Cette maladie se manifeste initialement par un essoufflement à l’effort qui limite de plus en plus les patients. Un essoufflement inexpliqué doit donc conduire à un avis spécialisé en pneumologie ou cardiologie et à envisager une échographie du cœur.
Vos travaux ont permis de mieux comprendre les mécanismes inflammatoires et génétiques impliqués dans l’HTAP. Quels sont-ils ?
L’HTAP est parfois une maladie familiale et il a fallu de nombreuses années pour identifier les gènes impliqués, au premier rang desquels figure le gène BMPR2. Au niveau des vaisseaux pulmonaires, BMPR2 joue un rôle essentiel dans le contrôle de la prolifération cellulaire et le maintien d’un équilibre vasculaire pulmonaire harmonieux. Mes travaux s’inscrivaient depuis longtemps dans l’étude des mécanismes inflammatoires ainsi que des bases cellulaires et moléculaires du remodelage vasculaire pulmonaire. Dans l’HTAP, l’augmentation de la pression dans les artères pulmonaires ne résulte pas d’une simple contraction des vaisseaux, mais surtout d’un processus d’obstruction progressive lié à une prolifération excessive de la paroi vasculaire. Sur le plan physiologique, la circulation pulmonaire repose sur un équilibre permanent entre des signaux qui freinent la prolifération, largement transmis par la voie BMPR2, et d’autres signaux qui la stimulent, notamment la voie de l’activine, sur laquelle mon équipe travaille également depuis de nombreuses années. Lorsque BMPR2 est muté, les signaux inhibiteurs diminuent, laissant la voie de l’activine prédominer et favoriser le remodelage vasculaire. Nous avons montré que l’HTAP associe non seulement des anomalies de la voie BMPR2, fréquentes dans les formes familiales, mais aussi des anomalies de la voie de l’activine. Ces travaux ont conduit au développement d’un biomédicament, le sotatercept, qui agit en piégeant l’activine. En réduisant son action au niveau des vaisseaux pulmonaires, il permet de limiter la prolifération vasculaire et de diminuer la pression dans les artères pulmonaires, ouvrant ainsi une nouvelle voie thérapeutique.
Comment les progrès thérapeutiques ont-ils modifié le pronostic et la qualité de vie des patients atteints d’HTAP ?
Dans les années 1980 et 1990, des découvertes ont permis de montrer que des molécules comme la prostacycline, le monoxyde d’azote ou l’endothéline, permettent de dilater ou de contracter les artères pulmonaires, ce qui a permis le développement de médicaments vasodilatateurs. Avant le sotatercept, ces trois grandes voies thérapeutiques étaient les seules ciblées pour le traitement de l’HTAP. Initialement testées seules, ces voies thérapeutiques ont été rapidement utilisées de façon combinée, les malades recevant généralement deux ou trois médicaments vasodilatateurs. Le sotatercept est un traitement supplémentaire qu’on ajoute à ces autres médicaments. En plus des traitements médicamenteux, la transplantation pulmonaire reste une option indispensable pour certains patients dont la maladie est résistante au traitement médicamenteux maximal. Plus rarement, une transplantation cœur-poumon peut même être envisagée. Grâce aux progrès thérapeutiques, une meilleure connaissance de la maladie et une meilleure organisation des soins, notamment avec le développement de centres de référence et de centres de compétence dédiés à l’HTAP sur l’ensemble du territoire, le pronostic de la maladie a profondément évolué. Alors qu’il y a trente ans l’espérance de vie était inférieure à trois ans après le diagnostic, elle dépasse aujourd’hui largement six ans en moyenne, et de nombreux patients vivent bien plus de dix ans avec la maladie. Il reste de nombreux défis : certains patients sont réfractaires aux traitements actuels, ce qui rend indispensable le maintien de la possibilité de recourir à la transplantation pulmonaire. Par ailleurs, il est essentiel de poursuivre la recherche afin de découvrir de nouvelles voies thérapeutiques pour mieux contrôler la pression dans les artères pulmonaires.
Vous avez contribué à construire l’un des plus grands registres mondiaux de patients, avec plus de 20 000 cas suivis. Pouvez-vous nous expliquer en quoi ces registres sont indispensables ?
Les registres font partie des outils essentiels à l’étude des maladies rares. Ces bases de données nous permettent de savoir quelle est l’histoire naturelle de la maladie, comment elle évolue, répond aux traitements, quels sont les maladies associées et les facteurs de risque mais aussi l’épidémiologie de la maladie. Un autre outil intéressant est constitué par les biobanques, banques de matériels biologiques avec du plasma, du sérum, de l’ADN, des tissus pulmonaires, qui nous permettent de mieux comprendre les mécanismes de cette maladie. Les réseaux de soins sont indispensables car il faut suffisamment de malades pour bien comprendre une maladie et aussi offrir la meilleure qualité des soins au plus près du patient. Le réseau PulmoTension offre aux malades un centre expert de l’HTAP à moins de deux heures de route de chez eux. Sur le plan européen, le réseau de référence ERN-LUNG permet de développer un réseau de soins très puissant. Notre centre de référence peut ainsi former des cardiologues et des pneumologues dans toute l’Europe et au-delà. Cette transmission de la connaissance est un grand succès dans le domaine des maladies rares.
Vous insistez souvent sur la dimension humaine de la recherche. Qu’est‑ce qui vous motive au quotidien ?
On ne fait pas de la recherche médicale par hasard mais avant tout pour aider des patients, parfois très jeunes et en grande difficulté. J’ai commencé à travailler sur cette maladie parce que je voyais des patients atteints d’une pathologie inexplicable et souvent mortelle. Avec eux, se construit une relation forte, presque amicale, autour d’un objectif commun : trouver des moyens de mieux traiter, et un jour, de guérir cette maladie. Lors d’un congrès que nous avons récemment organisé aux États-Unis, j’ai souhaité que des patients prennent la parole. Ce moment a été particulièrement émouvant. L’une d’elles a raconté que, lorsqu’on lui a annoncé le diagnostic d’HTAP, elle a immédiatement pensé à la mort. Dix ans plus tard, grâce aux avancées de la recherche et à l’engagement des patients eux-mêmes, désormais organisés en réseaux, sa première pensée le matin n’est plus la fin, mais cette question pleine d’avenir : « Que ferai-je dans dix ans ? »
Propos recueillis par Anne-Sophie Glover-Bondeau